Статья опубликована в рамках: XXXVIII Международной научно-практической конференции «Естественные и математические науки в современном мире» (Россия, г. Новосибирск, 13 января 2016 г.)
Наука: Химия
Секция: Биоорганическая химия
Скачать книгу(-и): Сборник статей конференции
дипломов
Статья опубликована в рамках:
Выходные данные сборника:
КОМПОНЕНТНЫЙ СОСТАВ И БИОЛОГИЧЕСКАЯ АКТИВНОСТЬ ЭФИРНОГО МАСЛА TANACETUM VULGARE L. ИЗ ВОСТОЧНОГО КАЗАХСТАНА
Мухтарова Акерке Балжанкызы
магистрант по специальности «ХТОВ», Казахский университет технологии и бизнеса,
Республика Казахстан, г. Астана
Искакова Жанар Бактыбаевна
канд. хим. наук, ведущий научный сотрудник института прикладной химии ЕНУ им. Л.Н. Гумилева,
Республика Казахстан, г. Астана
Cүлеймен Ерлан Мэлсұлы
канд. хим. наук, PhD, директор института прикладной химии, доц. кафедры химии ЕНУ им. Л.Н. Гумилева,
Республика Казахстан, г. Астана
Ибатаев Жаркын Абыкенович
канд. хим. наук, ведущий научный сотрудник института прикладной химии ЕНУ им. Л.Н. Гумилева,
Республика Казахстан, г. Астана
Мырзагалиева Анар Базаровна
д-р биол. наук, проф., проректор по УМР ВКГУ им. С. Аманжолова,
Республика Казахстан, г. Оскемен
Медеубаева Балжан Заруетовна
магистр химии, старший преподаватель кафедры химии ВКГУ им. С. Аманжолова,
Республика Казахстан, г. Оскемен
CHEMICAL COMPOSITION AND BIOLOGICAL ACTIVITY OF TANACETUM VULGARE L. ESSENTIAL OILS FROM EAST KAZAKHSTAN
Akerke Muhtarova
master's student, specialty “Chemical technology of organic substances”
of Kazak University of Technology and Business,
Kazakstan, Astana
Zhanar Iskakova
candidate of Chem. Science, Leading Researcher of the Institute of Applied Chemistry of ENU,
Kazakstan, Astana
Yerlan Suleimen
candidate of Chem. Science, PhD, Director of the Institute of Applied Chemistry of ENU,
Associate Professor of Chemistry Department of L. N. Gumilev ENU,
Kazakstan, Astana
Zharkyn Ibatayev
candidate of Chem. Science, Leading Researcher of the Institute of Applied Chemistry of ENU,
Kazakstan, Astana
Anar Myrzagaliyeva
doctor of biological sciences, Professor,
Vice-rector for academic and educational work of S. Amanzholov EKSU,
Kazakstan, Oskemen
Balzhan Medeubayeva
master of chemistry, Senior teacher of department of chemistry S. Amanzholov EKSU,
Kazakstan, Oskemen
АННОТАЦИЯ
Проведено изучение компонентного состава, цитотоксической и антирадикальной активности эфирного масла Tanacetum vulgare L., произрастающего в Восточно-Казахстанской области Казахстана.
ABSTRACT
The composition, cytotoxic and antiradical activity of Tanacetum vulgare L. essential oil from East Kazakhstan region of Kazakstan were studied.
Ключевые слова: Tanacetum vulgare L.; эфирное масло, компонентный состав; ГХ/МС; цитотоксическая активность; Artemia salina, антирадикальная активность; DPPH.
Keywords: Tanacetum vulgare L.; essential oil; composition; GC/MS; cytotoxic activity; Artemia salina; antiradical activity; DPPH.
Tanacetum vulgare L. (пижма обыкновенная, сем. Asteraceae Dumort.) – многолетнее травянистое растение, высотой 50–150 см. Растению присущ характерный (камфорный) запах. Произрастает на всей территории Европы, в России, Турции, Казахстане, Киргизии, Монголии, Китае, Японии и Корее. Встречается почти во всех районах Казахстана, кроме южных пустынь [3].
Целью работы явилось определение химического состава, а также изучение цитотоксической и антирадикальной активности эфирного масла растения T. vulgare из Восточного Казахстана.
Эфирное масло T. vulgare проявляет широкий спектр биологической активности [1; 6; 7]. Компонентный состав и степень биологической активности эфирного масла зависит от многих факторов, главным из которых является география произрастания растения [4; 8–10; 12].
Исходное сырье собирали на хребте Ивановский Рудного Алтая в первой декаде августа 2014 г. На Ивановском хребте T. vulgare распространена повсеместно: по кустарникам, полям, по лугам и луговым степям в разнотравных, разнотравно-злаковых и разнотравно-пижмовых ассоциациях.
Эфирное масло получали методом гидродистилляции на аппарате Клевенджера в течение 2-х часов. Прибор предназначен для определения содержания эфирного масла в растительном сырье по методу Клевенджера, путем перегонки его с водяным паром и последующего измерения объема полученного масла, выраженного в процентах по отношению к абсолютно сухому сырью [2]. Для получения эфирного масла была использована надземная часть растения. Выход эфирного масла составил 0,2 %.
Определение компонентного состава эфирного масла проводили на газовом хроматографе Clarus-SQ 8 (PerkinElmer) с масс-спектрометрическим детектором (рис. 1).
Приготовление пробы эфирного масла: около 25 мг (точная навеска) эфирного масла T. vulgare помещали в мерную колбу вместимостью 25 мл, растворяли в 15 мл гексана, доводили до метки и перемешивали до полного смешения масла.
Хроматографические условия: колонка капиллярная RestekRxi®-1 ms 0,25 мм х 30 м х 0,25 мкм, объем пробы: 1,0 мкл, газ-носитель Не, скорость газа-носителя: 1 мл/мин, деление потока 1:25, t колонки: 40ºС, подъем 2 С/мин до 280оС, t испарителя – 280оС, масс-спектрометрический детектор: t – 240оС, EI+ = 70 eB, время сканирования с 4 по 120 мин, режим сканирования ионов 39–500 m/z. Процентное содержание компонентов вычисляли автоматически, исходя из площадей пиков общей хроматограммы ионов. Компоненты идентифицировали по масс-спектрам и времени удерживания, с использованием библиотеки NIST.
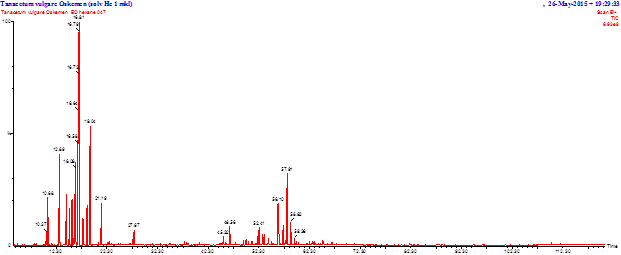
Рисунок 1. Хроматограмма эфирного масла T. vulgare
Таблица 1.
Компонентный состав эфирного масла T. vulgare
|
ВУ |
Название компонента |
Содержание % |
|
10,372 |
β-Туйон |
0,5 |
|
10,68 |
α-Пинен |
1,9 |
|
12,893 |
Сабинен |
4,0 |
|
12,995 |
β-Пинен |
0,4 |
|
14,287 |
β-Мирцен |
2,5 |
|
14,91 |
α-Фелландрен |
2,2 |
|
15,464 |
3-Карен |
2,5 |
|
15,828 |
α-Терпинен |
0,4 |
|
16,114 |
o-Цимол |
8,0 |
|
16,785 |
β-Фелландрен |
22,7 |
|
16,85 |
β-Терпинен |
3,4 |
|
17,578 |
trans-β-Оцимен |
1,3 |
|
18,381 |
cis-β-Оцимен |
2,3 |
|
19,041 |
γ-Терпинен |
10,5 |
|
21,191 |
Лимонен |
2,3 |
|
22,538 |
2-Метилбутил-2-метилбутаноат |
0,2 |
|
22,835 |
2-Метилбутилизовалериат |
0,3 |
|
23,21 |
cis-Сабинен гидрат |
0,1 |
|
27,344 |
Лавандиол |
0,3 |
|
27,67 |
Терпинен-4-ол |
1,0 |
|
37,583 |
trans-Сабинилацетат |
0,2 |
|
38,053 |
Лавандиолацетат |
0,2 |
|
45,317 |
a-Копаен |
0,6 |
|
45,761 |
β-Баурбонен |
0,2 |
|
46,561 |
β-Елемен |
1,2 |
|
49,217 |
Геранилизобутират |
0,3 |
|
49,811 |
γ-Елемен |
0,4 |
|
50,266 |
α-Гвайэн |
0,3 |
|
50,912 |
Гумулен |
0,3 |
|
52,159 |
trans-β-Фарнезен |
0,9 |
|
52,409 |
Лавандулилизобутират |
1,1 |
|
53,043 |
Гремакрен D |
0,7 |
|
53,366 |
β-Селинен |
0,7 |
|
54,221 |
α-Селинен |
0,6 |
|
54,808 |
Аромандендрен |
0,3 |
|
56,393 |
Аристолен |
0,2 |
|
57,127 |
Валенсен |
1,4 |
|
57,523 |
β-Маалиен |
0,3 |
|
57,908 |
(2E, 6E)-Фарнезилпентаноат |
9,7 |
|
58,62 |
Гермакрен B |
1,5 |
|
59,361 |
Геранилангелат |
0,4 |
|
59,684 |
trans-Неролидол |
0,2 |
|
60,073 |
Юненол |
0,2 |
|
62,277 |
Изоспатуленол |
0,3 |
|
62,901 |
Кубебол |
0,2 |
|
63,202 |
Аристол-1(10)-ен-9-ол |
0,2 |
|
64,868 |
3,5,11-Еудесматриен |
0,3 |
|
65,062 |
β-Гвайен |
0,2 |
|
Всего |
89,8 |
|
Анализ табличных данных показывает, что эфирное масло T. vulgare состоит из различных монотерпеноидов (67 %) и сесквитерпеноидов (22,7 %). Основными компонентами эфирного масла являются β-фелландрен (22,7 %), (2E, 6E)-фарнезилпентаноат (9,7 %), о-цимол (8,0 %), сабинен (4,0 %) и β-терпинен (3,4 %).
Изучение цитотоксической активности проводили по методике описанной нами в [5]. Проводили исследования цитотоксичной активности эфирного масла T. vulgare на рачках Artemia salina. В качестве контроля использовали раствор диметилсульфоксида. Готовили образцы эфирного масла следующих концентраций: 10,0; 5,0 и 1 мг/мл (таблицы 2–4).
Таблица 2.
Эфирное масло T. vulgare 10 мг/мл
|
Параллель |
К-во личинок в контроле |
К-во личинок в образце
|
% вы-живших личинок в контроле |
% выживших личинок в образце |
Смерт-ность, А,% |
Наличие нейро-токсич-ности, % |
|||
|
выж. |
погиб. |
выж |
погиб. |
пар. |
|||||
|
1 |
23 |
1 |
0 |
20 |
0 |
96 |
0 |
96 |
0 |
|
2 |
21 |
2 |
0 |
28 |
0 |
||||
|
3 |
24 |
1 |
0 |
24 |
0 |
||||
|
Ср |
23 |
1 |
0 |
24 |
0 |
||||
Таблица 3.
Эфирное масло T. vulgare 5 мг/мл
|
Параллель |
К-во личинок в контроле |
К-во личинок в образце
|
% вы-живших личинок в контроле |
% выживших личинок в образце |
Смерт-ность, А,% |
Наличие нейро-токсич-ности, % |
|||
|
выж. |
погиб. |
выж |
погиб. |
пар. |
|||||
|
1 |
23 |
1 |
0 |
20 |
0 |
96 |
0 |
96 |
0 |
|
2 |
21 |
2 |
0 |
24 |
0 |
||||
|
3 |
24 |
1 |
0 |
20 |
0 |
||||
|
Ср |
23 |
1 |
0 |
21 |
0 |
||||
Таблица 4.
Эфирное масло T. vulgare 1 мг/мл
|
Параллель |
К-во личинок в контроле |
К-во личинок в образце
|
% вы-живших личинок в контроле |
% выживших личинок в образце |
Смерт-ность, А,% |
Наличие нейро-токсич-ности, % |
|||
|
выж. |
погиб. |
выж |
погиб. |
пар. |
|||||
|
1 |
23 |
1 |
0 |
16 |
8 |
96 |
0 |
69 |
27 |
|
2 |
21 |
2 |
0 |
15 |
5 |
||||
|
3 |
24 |
1 |
0 |
18 |
4 |
||||
|
Ср |
23 |
1 |
0 |
16 |
6 |
||||
Исследования показали, что эфирное масло T. vulgare L. в концентрациях 10 и 5 мг/мл проявляют острую летальную токсичность – все личинки погибают. Смертность личинок морских рачков в концентрации 1 мг/мл составляет 69 %, а остальная часть, то есть 27 % личинок находились в парализованном состоянии.
Продолжая исследование объекта нами изучена антирадикальная активность (АРА) полученного эфирного масла T. vulgare L.
Антирадикальная активность определена с помощью реакций ингибирования 2,2-дифенил-1-пикрилгидразилрадикала (DPPH) [11]. Антирадикальную активность исследуемых объектов определяли по формуле:
АРА (%) = (A0 – At)/ A0 *100 (1)
где: A0 – оптическая плотность контрольного образца;
At – оптическая плотность рабочего образца.
Оптическую плотность исследуемых растворов, зависимую от концентрации измеряли на спектрофотометре Cary 60 UV-Vis при длине волны 520 нм.
Рассчитанные по формуле (1) значения АРА эфирного масла растения приведены в таблице 5.
Таблица 5.
Антирадикальная активность (%) эфирного масла растений T. vulgare L. при разных концентрациях
|
№ |
Исследуемые вещества |
Концентрация экстрактов (мг/мл) |
||||
|
0,1 |
0,25 |
0,5 |
0,75 |
1,0 |
||
|
1 |
Бутилгидроксианизол (ВНА) |
80,82 |
81,23 |
80,30 |
83,08 |
83,88 |
|
2 |
Эфирное масло Tanacetum vulgare L. |
8,37 |
10,72 |
12,38 |
13,15 |
13,45 |

Рисунок 2. Динамика антирадикальной активности при изменении концентрации веществ
На основании анализа данных таблицы 5 и графика видно, что эфирное масло T. vulgare L. имеет низкую антирадикальную активность по сравнению с бутилгидроксианизолом.
Таким образом в ходе проведенных исследований нами был установлен компонентный состав эфирного масла T. vulgare L из Восточного Казахстана. Эфирное масло T. vulgare L. главным образом содержит следующие компоненты: β-фелландрен (22,7 %), (2E, 6E)-фарнезилпентаноат (9,7 %), о-цимол (8,0 %), сабинен (4,0 %) и β-терпинен (3,4 %). Изучение биологической активности показало, что эфирное масло T. vulgare L. проявляет летальную токсичность и обладает низкой антирадикальной активностью.
Список литературы:
1. Айсабаева Е.О., Ефанова А.Б., Савченко Т.С., Янилкин В.В., Настапова Н.В., Племенков В.В. Антиоксидантная способность эфирных масел растений // Химия и технология растительных веществ: VII Всероссийская научная конференция. – Сыктывкар, – 2011. – С. 15.
2. Государственная Фармакопея СССР. Вып. 2. Общие методы анализа. Лекарственное растительное сырье МЗ СССР. 11-еизд. – М., 1990. – С. 400.
3. Губанов И.А., Киселева К.В., Новиков В.С., Тихомиров В.Н. Иллюстрированный определитель растений Средней России. Том 3. Покрытосеменные (двудольные: раздельнолепестные), 2004. – С. 493.
4. Мильшина Л.А., Ефремов А.А., Первышина Г.Г. Влияние абиотических факторов окружающей среды на компонентный состав эфирного масла пижмы обыкновенной (Tanacetum vulgare L.). Вестник КрасГАУ. – 2010. – № 8. – С. 139–143.
5. Сүлеймен Е.М. Компоненты Peusedanum morisonii Bess. и их антимикробная и цитотоксическая активность. Химия природ. соедин., 2009. – 45 (5). – С. 710–711.
6. Хусаинова А.И. Фармакогностическое исследование цветков пижмы обыкновенной (Tanacetum vulgare L.). Диссертация…канд. фарм. наук. Самара: СГМУ, 2015. – С. 206.
7. Kumar V., Tyagi D. Chemical Composition and Biological Activities of Essential Oils of Genus Tanacetum – a review. Journal of Pharmacognosy and Phytochemistry. – 2013. – 2. – P. 159–163.
8. Mockute D., Judzentiene A. The myrtenol chemotype of essential oil of Tanacetum vulgare L. var. vulgare (tansy) growing wild in the Vilnius region. Chemija. – 2003. – 14 (2). – P. 103–107.
9. Piras A., Falconieri D., Bagdonaite E., Maxia A., Gonçalves M.J., Cavaleiro C., Salgueiro L., Porcedda S. Chemical composition and antifungal activity of supercritical extract and essential oil of Tanacetum vulgare growing wild in Lithuania. Natural Product Research. – 2014. – 28 (21). – P. 1906–1909.
10. Raal A., Orav A., Gretchushnikova T. Essential Oil Content and Composition in Tanacetum vulgare L. Herbs Growing Wild in Estonia. Journal of Essential Oil Bearing Plants. – 2014. – 17 (4). – P. 670–675.
11. Sawant O., Kadam V.J., Ghosh R. In vitro Free Radical Scavenging and Antioxidant Activity of Adiantum Lunulatum. Journal of Herbal Medicine and Toxicology. – 2009. – 3 (2). – P. 39–44.
12. Szolyga B., Gnilka R., Szczepanik M., Szumny A. Chemical composition and insecticidal activity of Thuja occidentalis and Tanacetum vulgare essential oils against larvae of the lesser mealworm, Alphitobius diaperinus. Entomologia Experimentalis et Applicata. – 2014. – 151 (1). – P. 1–10.
дипломов


Оставить комментарий